
Quando l’AI fa davvero la differenza: 5 svolte concrete in medicina
L’intelligenza artificiale viene spesso raccontata come “il futuro della medicina”.
La verità è che in molti ambiti è già presente e operativa, anche in tempi non sospetti, e sta migliorando diagnosi, terapie e processi clinici in modo tangibile e misurabile.
In questo articolo abbiamo raccolto 5 casi significativi e documentati in cui l’AI ha rappresentato una svolta, con riferimenti a studi e implementazioni tecniche.
1. Diagnosi precoce dei tumori grazie all’imaging basato su AI
L’imaging radiologico è uno dei settori dove l’intelligenza artificiale ha avuto impatti concreti e immediati. Un gruppo di ricerca guidato dalla Mayo Clinic ha dimostrato che l’AI può individuare segnali precoci di tumore al pancreas su TAC addominali anche fino a 3 anni prima rispetto alla diagnosi clinica standard. Il modello è stato addestrato su decine di migliaia di immagini di pazienti, riuscendo a riconoscere pattern impercettibili all’occhio umano.
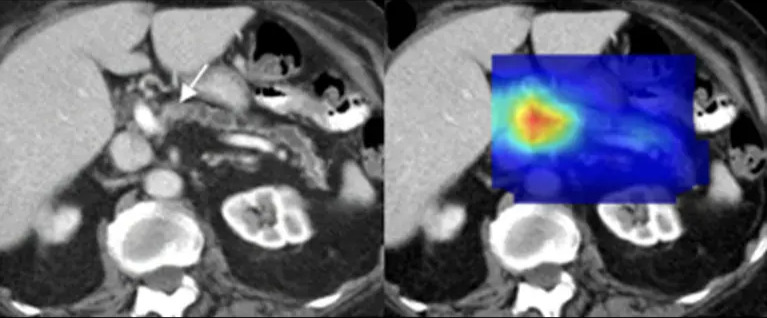
Uno studio parallelo pubblicato su SpringerLink ha mostrato come l’intelligenza artificiale possa aumentare la sensibilità diagnostica in radiologia toracica e neuroradiologica, migliorando ad esempio l’identificazione di noduli polmonari e lesioni compatibili con la sclerosi multipla.
Angolo nerd
Questi sistemi si basano su modelli di deep learning progettati per leggere immagini mediche. In particolare, reti neurali convoluzionali (CNN) 2D e 3D vengono addestrate su grandi dataset di TAC annotate per riconoscere pattern morfologici complessi a livello di pixel, in modo analogo al lavoro di un radiologo ma con una granularità molto più fine. Architetture di tipo U-Net vengono utilizzate per la segmentazione semantica, cioè per isolare automaticamente le aree potenzialmente patologiche. Il risultato non è una semplice classificazione sì/no, ma heatmap integrate nei sistemi PACS che indicano dove il modello concentra la propria attenzione. Le prestazioni vengono valutate con metriche orientate allo screening, come AUC, sensibilità e tasso di falsi negativi, particolarmente critiche quando l’obiettivo è individuare segnali precoci di malattia.
2. Predire l’Alzheimer prima dei sintomi clinici
Uno degli ambiti più promettenti dell’intelligenza artificiale in medicina è la predizione precoce delle malattie neurodegenerative, in particolare dell’Alzheimer. In questo caso il valore dell’AI non sta tanto nella diagnosi formale, quanto nella capacità di intercettare segnali deboli anni prima che il declino cognitivo diventi clinicamente evidente.
Diversi studi condotti negli Stati Uniti, tra cui ricerche della University of California San Francisco (UCSF), mostrano come modelli di machine learning possano stimare il rischio di sviluppare Alzheimer fino a 5–7 anni prima della comparsa dei sintomi, integrando dati clinici longitudinali, neuroimaging e biomarcatori.
In pratica, l’AI viene utilizzata per riconoscere pattern di progressione che, presi singolarmente, sarebbero poco significativi, ma che nel loro insieme raccontano una traiettoria di rischio.
Angolo nerd
I modelli più efficaci lavorano principalmente su dati longitudinali, ovvero informazioni raccolte nel tempo sullo stesso paziente. I modelli combinano algoritmi di machine learning supervisionato (come random forest e gradient boosting) per analizzare cartelle cliniche strutturate, con reti neurali profonde applicate a immagini di risonanza magnetica (MRI) o PET cerebrali. Quando l’obiettivo è stimare quando un paziente potrebbe sviluppare la malattia, entrano in gioco modelli di survival analysis potenziati dall’AI, capaci di associare un profilo di rischio a una finestra temporale. In studi più avanzati, anche segnali linguistici e cognitivi vengono integrati tramite modelli transformer per individuare alterazioni semantiche precoci.
3. Scoperta di nuovi farmaci con AI generativa
Nel 2020, il MIT ha fatto notizia con la scoperta di Halicin, un antibiotico completamente nuovo, individuato da un algoritmo AI che ha setacciato oltre 100 milioni di molecole note in pochi giorni. Pubblicato su Cell, lo studio ha mostrato come modelli generativi possano trovare soluzioni terapeutiche fuori dagli schemi tradizionali.
Allo stesso tempo, la biotech Insilico Medicine ha utilizzato due piattaforme proprietarie, PandaOmics e Chemistry42, per progettare e portare in fase clinica una molecola antifibrotica in meno di 30 mesi, contro una media industriale di 5–6 anni.
Angolo nerd
Nella drug discovery l’AI viene utilizzata per esplorare spazi chimici enormi, difficilmente gestibili con approcci tradizionali. Modelli generativi come variational autoencoder (VAE) o GAN apprendono la “grammatica” delle molecole e generano nuove strutture candidate, che vengono poi valutate tramite modelli predittivi (QSAR) e simulazioni di docking molecolare. L’ottimizzazione delle molecole può essere guidata da tecniche di reinforcement learning, che bilanciano più obiettivi contemporaneamente, come efficacia, tossicità, stabilità e sintetizzabilità. In questo modo l’AI non sostituisce il laboratorio, ma riduce drasticamente il numero di esperimenti necessari.
4. Chirurgia assistita da AI: più precisione, meno variabilità
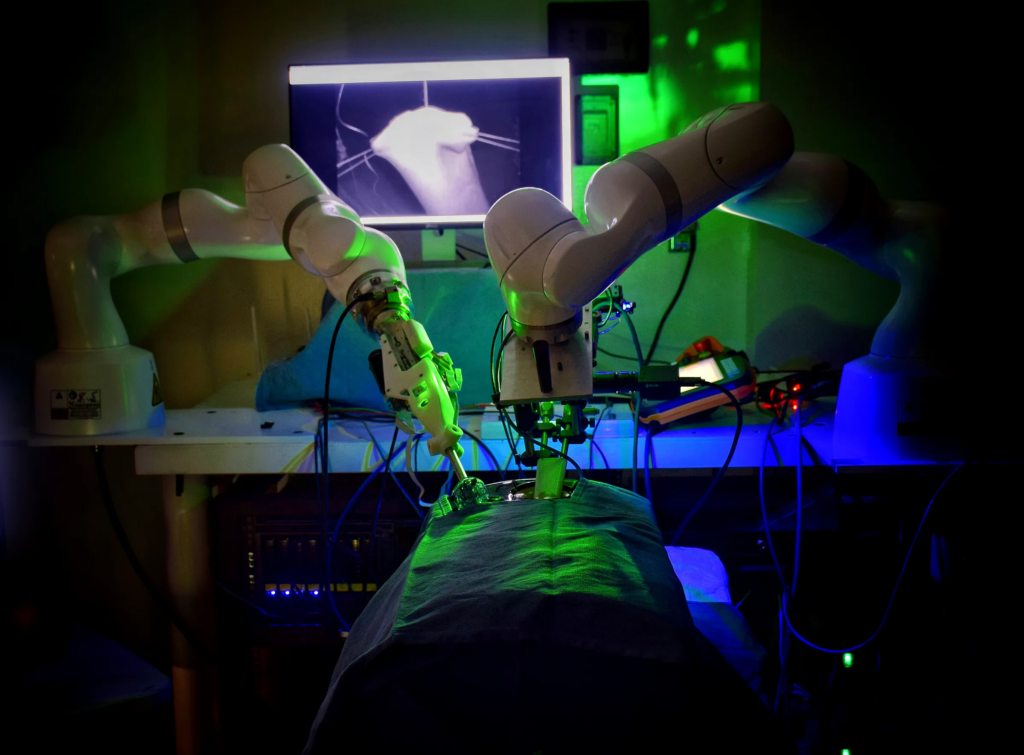
I sistemi robotici assistiti da AI stanno già trasformando la pratica chirurgica. Dispositivi come ROSA (per neurochirurgia e ortopedia) integrano imaging pre-operatorio, pianificazione personalizzata e feedback in tempo reale per aumentare la precisione. Ancora più innovativo è il caso del robot STAR, che ha eseguito suture su tessuti molli in autonomia, con prestazioni superiori a quelle di chirurghi umani secondo uno studio pubblicato su Science Translational Medicine.
Angolo nerd
Nei sistemi di chirurgia assistita, l’AI affronta il problema complesso di operare su un ambiente in continuo movimento. Per farlo, combina visione artificiale 3D, tracking del tessuto e modelli di pianificazione del movimento ispirati alle traiettorie chirurgiche umane. L’addestramento avviene su dataset di interventi reali, da cui il sistema apprende gesti, vincoli e variabilità. Durante l’operazione, algoritmi di controllo correggono le traiettorie in tempo reale sulla base di feedback visivi, di forza e, in alcuni casi, di imaging a fluorescenza, consentendo una sutura adattiva e più riproducibile.
5. Medicina personalizzata e casi complessi: decision support su base AI
In oncologia e nelle malattie rare, l’AI sta rivoluzionando l’approccio terapeutico. Il sistema ACMA (AI Case Matching Algorithm), presentato all’ASCO, analizza migliaia di cartelle cliniche, profili genetici e risposte ai trattamenti per suggerire opzioni terapeutiche personalizzate con una precisione superiore ai metodi tradizionali.
Un caso emblematico raccontato dal medico e divulgatore Bertalan Meskó riguarda un paziente affetto da una forma refrattaria di Malattia di Castleman: un algoritmo AI ha identificato un farmaco off-label che ha portato alla remissione del paziente, aprendo nuove prospettive nel trattamento di condizioni ultra-rare.
Angolo nerd
Nei sistemi di decision support clinico l’obiettivo non è solo fare previsioni, ma mettere in relazione informazioni eterogenee. Per questo vengono utilizzati modelli multimodali e approcci a grafo, in cui diagnosi, geni, farmaci, trattamenti e outcome sono rappresentati come nodi e relazioni. Tecniche come graph embeddings e graph neural networks permettono di identificare pattern e somiglianze tra casi clinici complessi, supportando il medico nel confrontare un paziente con migliaia di casi reali. Un requisito chiave è l’explainability: ogni raccomandazione deve essere tracciabile e giustificabile in un contesto clinico reale.
_Cosa impariamo dall’approccio medico all’AI
Questi casi dimostrano che l’AI in medicina non è più sperimentale: è una tecnologia abilitante, già oggi operativa in contesti ad alto impatto clinico.
Ma c’è un aspetto fondamentale che spesso viene sottovalutato: la qualità e la natura dei dati di addestramento fanno la vera differenza tra un’AI teoricamente promettente e una realmente utile nella pratica medica.
In ambito sanitario, i modelli non apprendono nel vuoto. Si addestrano su anni di pratica clinica umana, su immagini diagnostiche refertate da specialisti, su cartelle cliniche strutturate, su interventi chirurgici eseguiti e validati. Il robot STAR, ad esempio, non “impara da solo”: le sue capacità derivano dall’analisi di migliaia di suture eseguite da chirurghi, trasformate in dati, traiettorie e pattern riproducibili. Lo stesso vale per i sistemi di imaging, allenati su dataset annotati da radiologi, o per i modelli predittivi, che ereditano conoscenza clinica codificata nei dati storici.
È per questo che in medicina l’AI non sostituisce l’esperienza umana: la incorpora, la amplifica e la rende scalabile. Senza dati affidabili, rappresentativi e curati, anche l’algoritmo più avanzato resta sterile.
In Fyonda, crediamo in un’AI spiegabile, concreta e responsabile, costruita a partire da dati di qualità e progettata per supportare decisioni reali. La sfida non è solo tecnologica, ma culturale: integrare l’AI in modo etico, sicuro e sostenibile, rispettando il valore dell’esperienza umana da cui tutto ha origine.




